2025 年体外诊断行业疲软,热景生物却加速转向创新药,当年预亏超 2 亿元,股价最高却狂飙 11 倍。此前其靠新冠检测试剂海外业务大赚,后成立 「未来技术研究院」 布局创新药。公司笃定押注 FIC 新药,同时开多个管线。但其连续两年亏损,面对质疑,创始人林长青称资金不是问题,同时他认为监管突破是胜负手,期待监管改革更快一点。
每经记者|林姿辰 每经编辑|魏官红
2025 年体外诊断 (IVD) 行业持续疲软,前三季度超过 70% 的上市公司陷入亏损,多项关键指标创近年新低。身处该行业的很多企业都在收缩战线、力保现金流。
曾经靠新冠检测试剂海外业务大赚的热景生物 (688068.SH),却干了一件让同行看不懂的事——加速转向创新药。结果更是出人意料:公司 2025 年预亏约 2 亿元,股价最高却狂飙 11 倍。
「我最担心的不是没钱,而是管线跑得不够快。」 近日,热景生物创始人林长青接受了 《每日经济新闻》 记者专访。这位从 IVD 赛道 「跨界」 做创新药的企业家,正试图回答一个绕不开的问题:做检测的,能做好药吗?
手上拿了这么多现金,不投入研发也被人骂
2019 年 9 月 30 日,热景生物顶着 「科创板 IVD 第一股」 的光环上市。2020 年新冠肺炎疫情在全球暴发,热景生物在新冠检测试剂业务的带动下,次年公司账上的现金及现金等价物余额同比增长超 200%,达到 11.54 亿元,三年 (2020 年至 2022 年) 净利润总和超过 32 亿元。而在新冠肺炎疫情之前,热景生物的盈利水平只有千万元级别。
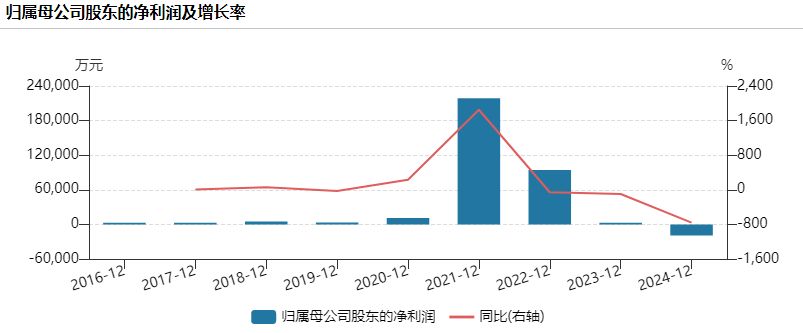
热景生物 2020 年至 2022 年累计净利润超过 32 亿元
图片来源:Wind 截图
2022 年以后,随着生产生活秩序回归日常,新冠检测试剂业务需求量大幅下滑。所有手握大把现金的 IVD 企业都在寻找新的业务增长点,有的同行直接 「买买买」,并购上下游企业,但林长青把目光落到了创新药项目上,牵头成立 「未来技术研究院」,布局抗体药物、核酸药物、活菌药物等生物制药领域前沿创新技术。
有人质疑热景生物蹭热度,创新药比 IVD 风险更大、周期更长;也有人认为当时不是投资创新药的好时候——2022 年,创新药一二级市场都处在寒冬中,不少初创企业陷入经营困境。
「我们为什么受大家关注呢?因为我们是从医疗器械,从体外诊断到创新药。」 林长青表示,许多创新药企是从传统的化药企业转型升级而来,但热景生物从体外诊断圈跳到药圈,是赛道里的 「非主流」。
但他也解释道,公司并不是在新冠肺炎疫情后突然转型,而是早就规划好了业务布局。体外诊断行业有局限性,只能诊断不做治疗,无法形成完整的商业闭环,而创新药能弥补这一短板,实现从诊断到治疗再到健康管理的全链条覆盖。
2018 年之前,林长青就在琢磨做创新药,直到港股的 18A 政策为尚未盈利的 Biotech(生物科技) 公司开了上市的口子,他才确定到了该出手的时候——2018 年年底,舜景医药注册成立,聚焦抗体药物研发。新冠肺炎疫情过后,主攻小核酸药物的尧景基因、布局生物技术消费品的禹景药业相继成立,共同构成热景生物的 「尧舜禹」 三大创新平台。
「说实话,当时 (新冠肺炎疫情之后) 手上拿了这么多现金,不投入研发也被人骂。」 在林长青看来,中国创新药崛起的历史性机遇已经到来,「如果一个企业长年累月的年利润只是两三千万元、三四千万元,给它 100 年也就赚 30 亿元,有什么意义?」
只做 FIC,不想 「又搞一把 PD-1 的内卷」
回过头来看,热景生物赶上了中国创新药的好时候。2023 年,泽布替尼的全球销售额为 91.38 亿元 (约 13 亿美元),成为首个年销售额超过十亿美元的国产创新药,让业内艳羡不已。最近两年,BD(商务拓展) 交易如火如荼,今年初,这份好运又落到了热景生物布局的小核酸赛道。
但创新药和医疗器械的研发逻辑不同,前者素有 「三个 10」 定律:10 亿美元投入、10 年时间、10% 成功率,而热景生物要做的靶点新、机制新的 FIC(同类首创) 新药,这一定律会被放得更大。
但林长青还是笃定,热景生物必须押注 FIC 创新药。此前,不少药企为了降低研发风险、加快上市速度,选择在海外已有创新药上市后,快速跟进研发同类产品。但这种 Fast Follow 模式也带来了严重的行业内卷,最典型的就是 PD-1 抑制剂,国内曾有超百家企业布局,最终引发价格战,产品商业价值大幅缩水。目前,除了 PD-1,GLP-1、ADC 等热门赛道也相继出现扎堆研发的情况,不少企业的产品尚未上市,就已面临激烈的市场竞争。
不过,FIC 带来的风险和资金投入也会更大。林长青表示,暂时的亏损不可怕,长期的落后才可怕。基本每家公司内部都有创新药管制委员会,会定期开会、梳理管线,有些立项时很领先,但后面可能落后,不得已会被砍掉。在国际市场上寻找授权合作时,冲在太前面的 FIC 还可能不如 Fast Follow, FIC 从感兴趣开始接触到深入理解再到被认可需要一个过程,但一旦被认可,收获将会非常可观,而且其相信,临床研究做得扎实、数据惊艳的 FIC 一定会被认可。
现在热景生物同时开了多个 FIC 管线。比如,舜景医药的 SGC001,是全球首个心梗治疗性抗体药,目前已在国内启动Ⅱ期临床试验;SGT003 精准靶向肿瘤微环境,是针对 X&CTLA-4 靶点的药物中全球首个进入临床的,2026 年启动临床研究Ⅰ期;尧景基因的心脏靶向递送平台 Kardia-ShuttleTM 避开了竞争激烈的肝内靶向,突破肝外递送这一技术瓶颈。
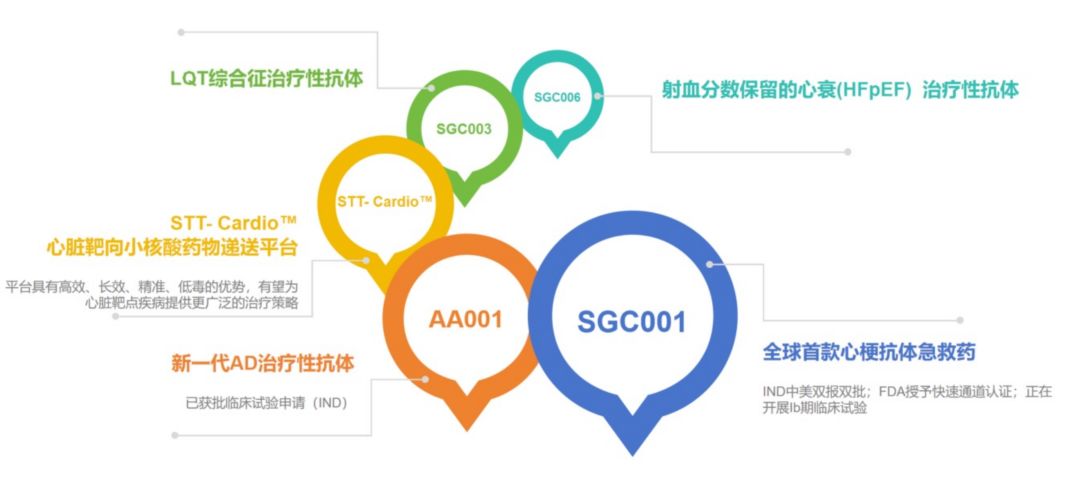
热景生物创新药板块第一产品方阵聚焦心脑血管
图片来源:受访者提供
但创新药的 「内卷」 程度肉眼可见。
「中国的创新药企业一拥而上,你如果做得慢一点,就可能卖不出去 (指海外权益授权),大家都在国内竞争,又搞了一把 PD-1 的内卷,是不是?」 林长青说。
年度业绩首次预亏超 2 亿元,「资金不是问题」
上市公司的定期财务数据,是交给投资者的成绩单。2 月 26 日,公司发布 2025 年度业绩快报,数据显示,热景生物全年实现收入 4.08 亿元,同比减少 20.20%;实现归母净利润-2.11 亿元,亏损同比扩大 10.22%,公司连续两年出现业绩亏损。
1 月中旬发布业绩预告时,公司曾表示,业绩变化受体外诊断行业集采等行业政策影响,净利润亏损扩大主要源于对创新药的战略投入。之后,公司股价从 214.78 元/股一路跌到不足 130 元/股。
仿佛一夜之间,热景生物的转型故事不灵了,投资者的质疑声也此起彼伏。
亏损超 2 亿元,股价最高反飙 11 倍 (2025 年),热景生物创新药神话是逆袭还是泡沫?
在不少人看来,即便前几年攒厚了家底,但创新药投资巨大,资金仍是热景生物未来面临的一大挑战。
林长青:「公司上市前,那时候我们担心的是资金,但是我们现在不担心。」
每经记者:「开了这么多 First-in-Class(FIC) 的项目,资金真的完全不担心了吗?」
林长青:「资金不是问题。」
林长青相信自己 「很敏锐地发现产业变化」,比如驱动创新药发展的资本,正在越来越 「友好」。基于此,公司可以充分利用资本市场进行融资,也可以借助海外 BD,让已有早期数据的管线价值提早变现,团队对后者寄予厚望,认为开发进度快、具有国际领先性的创新药管线,未来也有希望给集团带来可观的 BD 收入;只要产品足够有价值,不用担心资金的问题。
为此,今年 1 月,公司斥资赞助了 JPM 大会期间的 「2026 中国 FIC 创新与合作峰会」,带领 9 家国内创新药企到现场参与路演,这场中国创新药领域首次集中进行的 FIC 成果展示,吸引了辉瑞、葛兰素史克、吉利德、拜耳、默克、武田制药、百济神州、复宏汉霖、恒瑞医药、科伦博泰、RA Capital 等知名药企和投资机构到场。
「这些具有强大购买力的买方,都想来看中国的创新药数据。」 林长青说。
监管突破是胜负手,希望监管改革再快一点
从履历来看,林长青毕业于厦门大学生物系,29 岁离开万泰生物后创立了热景生物,在生物医药行业深耕多年,他经常和在美国实验室工作的同学们聊天,了解中国科研在全球坐标系中的最新位置。
2024 年 4 月,他回到自己攻读 EMBA 的清华大学做演讲,表示中国创新药将迎来爆发式增长的十年,这一预测很快得到验证——2025 年度中国创新药对外授权总金额首次突破 1000 亿美元,全球顶尖机构摩根士丹利发布研究报告,标题是 《中国 Biotech 创新药正迎来 「创新黎明」》。
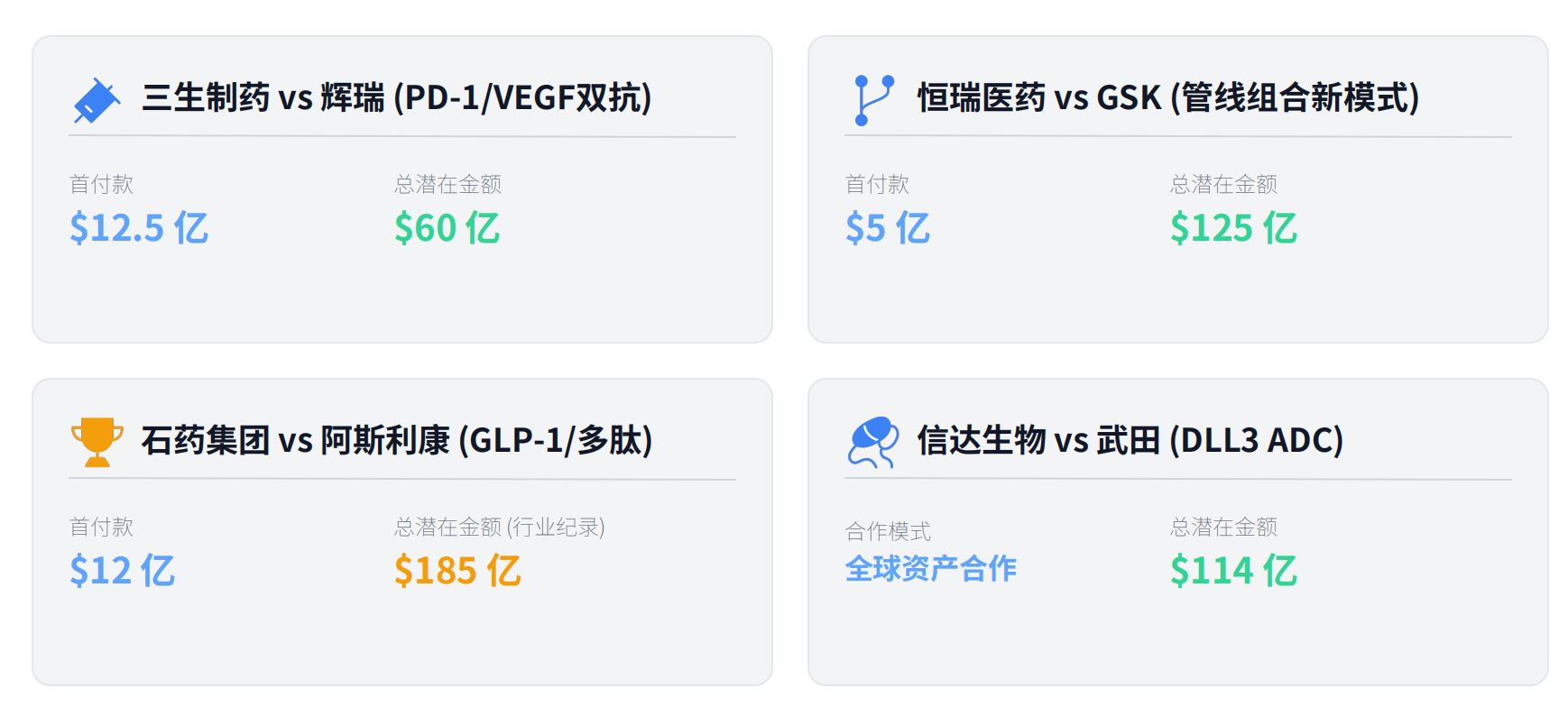
图片来源:受访者提供
在林长青看来,技术、政策和资本是驱动中国创新药发展的三股核心驱动力。在热景生物上市前,他自己最担心的是资金,但现在最关注的是政策,包括审评政策、商业化政策。
近年来,全球药品监管环境都在向好发展。作为全球药品审评审批风向标,FDA(美国食品药品监督管理局) 在去年 6 月推出 「局长国家优先审批券」(CNPV) 计划,药品研发人员可凭此券参与一项全新的优先审批计划,将 FDA 的审批时间从申请人最终提交药品申请后的大约 10 到 12 个月缩短至 1 到 2 个月。
中国的药监部门也在优化创新药临床试验审评审批,根据北京市连续两年发布的两版 《北京市支持创新医药高质量发展若干措施》,临床试验审批时限从 60 个工作日压缩至 30 个工作日,目前 14 个项目纳入试点,最快 18 个工作日获批,1 周启动临床试验。
这些变化让林长青感到振奋,但他还是有些担忧。FIC 创新药的核心优势在于其 「首创性」,可痛点也源于此——缺乏统一的行业标准,既没有明确的临床研究替代终点,也无统一的临床研究最终评价指标,更没有配套的临床指导原则,这就要求中国药监部门的审评工作必须跟上产业创新的步伐。
但是,国内的药品审批工作与 FDA 相比仍有较为明显差距。近年来,业内一直在讨论,监管层面亟待深化改革,是否要扩充审评专业人员队伍?是否需要建立适配创新药研发的全新审评机制?在临床替代终点的采纳、临床指导原则的制定、临床试验病例数的合理设定等具体环节,是否应该出台清晰的支持方案?
今年 1 月 6 日,国家药监局局长李利在全国药品监督管理工作会议上介绍工作部署,提到我国将对新机制、新靶点的创新药,在沟通交流、临床试验、注册申报、审评审批全链条强化服务支持,助力创新药 「中国首发」。
林长青还在等待更多的好消息,他始终担心管线跑得不够快——在这个烈火烹油的行业里,谁都怕自己起了个大早,赶了个晚集。
文章转载自 每经网