每经记者|林姿辰 每经编辑|段炼 董兴生
10 月 8 日晚间,A 股创新药龙头诺诚健华宣布了公司今年的第二笔 BD(商务拓展)。
根据公告,公司在美国的全资附属公司 InnoCare 与一家美国生物制药公司 Zenas 达成授权许可协议,Zenas 将获得诺诚健华核心产品——奥布替尼在多发性硬化领域的全球开发和商业化权益,以及奥布替尼在非肿瘤的其他治疗领域的开发与商业化权益。
此外,Zenas 还获得两款临床前分子,即一款新型口服 IL-17 AA/AF 抑制剂和一款透脑性口服 TYK2 抑制剂的相关权益。
为此,Zenas 将向诺诚健华支付达 1 亿美元的首付款和近期里程碑付款,包括 2026 年达成的里程碑付款,以及向诺诚健华发行达 700 万股 Zenas 普通股股票,包括在 2026 年初达到里程碑时向诺诚健华发行的股票。加上其他达成临床开发、注册和商业化里程碑的付款,潜在总交易金额超过 20 亿美元。此外,诺诚健华有权就授权产品的年度净销售额收取最高达高百分之十几的分级特许权使用费。
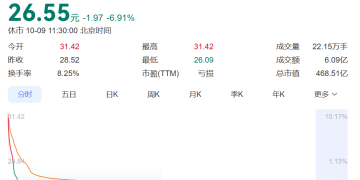
10 月 9 日,诺诚健华股价开盘跳水,截至中午收盘,其 A 股股价跌近 7%,港股股价跌近 10%。不过,年初至今其 A 股和港股股价均已翻倍。

保留核心产品肿瘤领域权利
2025 年是中国创新药企业的 BD 大年,此次诺诚健华将奥布替尼及 2 项临床前资产有偿许可给 Zenas,已经是公司今年达成的第二笔 BD,且延续了首笔 BD「绑定股权」 的形式。
在交易标的中,BTK 抑制剂奥布替尼是公司的核心产品,目前在国内获批 3 项适应证均聚焦在血液肿瘤领域,分别是复发/难治性套细胞淋巴瘤 (R/R MCL)、复发/难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 (R/R CLL/SLL) 和一线治疗慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 (CLL/SLL)。
在自身免疫性疾病领域,奥布替尼治疗原发进展型多发性硬化 (PPMS) 的 III 期注册临床试验已经启动,治疗继发进展型多发性硬化 (SPMS) 的 III 期注册临床试验预计 2026 年第一季度启动。
而本次诺诚健华与 Zenas 达成的授权范围,只涵盖了多发性硬化领域的全球权益,以及所有非肿瘤治疗领域,这意味着公司仍保留奥布替尼在肿瘤领域的全球独家权利,形成肿瘤自研、自免授权的双线布局。
另外,新型口服 IL-17 AA/AF 抑制剂、透脑性口服 TYK2 抑制剂均处于临床前阶段,目前还没有明确适应证,但参照已获批同类药物,两款药物在银屑病、银屑病关节炎等自身免疫性疾病领域发挥作用。
这也与 Zenas 的主攻领域吻合。资料显示,Zenas 于去年 9 月在纳斯达克证券交易所挂牌上市,聚焦自身免疫性疾病领域,现有产品均处于临床阶段。除了奥布替尼,公司的主要候选药物 Obexelimab 是一款双功能单克隆抗体,公司预计在今年第四季度公布 Obexelimab 治疗复发型多发性硬化 (RMS)MoonStone II 期临床试验 12 周的主要终点顶线数据,并于明年第一季度发布 24 周数据。
对于本次与诺诚健华的合作,Zenas 创始人兼首席执行官 Lonnie Moulder 表示,奥布替尼具有成为 best-in-class(同类最佳) 创新药的潜力,另外两款药物则是潜在 best-in-class 分子,公司预计 2026 年提交新药临床试验 (IND) 申请,并启动 I 期临床开发,并预计 2027 年获得口服 IL-17AA/AF 抑制剂的初始患者临床数据。

多发性硬化的全球权益系二次授权
早在 2021 年,诺诚健华曾与渤健就奥布替尼达成合作,约定将奥布替尼在 MS 领域的全球独家权利、除中国以外区域内的某些自身免疫性疾病领域的独家权利授予渤健。不过在 2023 年,渤健决定为便利而终止 (Terminate for Convenience) 双方此前达成的合作和许可协议,该项合作就此结束。
此次诺诚健华再次将奥布替尼的相关全球权益转让,全球 BD 风向已经发生巨大变化。9 月下旬,曾有国内公司创始人对记者表示,国外企业对中国药物试验数据的态度发生了积极的转变,BD 不是 「卖产品」,而是企业谋求出海的共赢手段。
从市场前景看,诺诚健华此次转让的三款自免管线各有价值。其中,多发性硬化在亚洲和非洲国家发病率整体较低,欧美市场更大。奥布替尼的 III 期注册临床试验针对的 PPMS 分型,仅奥瑞利珠单抗一款产品获批,存在较大未满足临床需求。
根据开源证券 7 月研报,全球范围内布局 MS 适应证进度较快的 BTK 抑制剂共有 5 款,其中默克的 Evobrutinib 因疗效不足及安全性问题已停止开发。诺诚健华的奥布替尼在激酶选择性、靶点亲和力、结合率与半衰期上均展现出优势,具有较强的临床开发潜力。
新型口服 IL-17 AA/AF 抑制剂则切入了剂型痛点,目前,以司库奇尤单抗为代表的全球畅销的 IL-17 抗体药物需要注射给药,部分患者存在用药抵触。另外,透脑性口服 TYK2 抑制剂的机理适用于银屑病等适应证,目前全球只有 1 款口服的选择性 TYK2 抑制剂获批,即 2022 年在美国获批的百时美施贵宝的 Sotyktu。
不过,创新与风险并存。比如,口服 IL-17 抑制剂的研发面临药物稳定性、生物利用度、胃肠道吸收等挑战,目前已经成为众多药企努力的目标,其中也包括中国药企——今年 5 月,歌礼制药宣布其用于治疗银屑病的口服小分子 IL-17 抑制剂 ASC50 的临床试验申请获得 FDA(美国食品药品监督管理局) 批准。
这对诺诚健华的资金实力提出了要求。记者注意到,截至 2025 年 6 月 30 日,公司持有现金及相关账户结余约 76.8 亿元,在生物科技公司中,诺诚健华资金储备较为充足。
(声明:文章内容 和数据仅供参考,不构成投资建议。投资者据此操作,风险自担。)
记者|林姿辰
编辑|段炼 董兴生 杜波
校对|陈柯名
 |每日经济新闻 nbdews 原创文章|
|每日经济新闻 nbdews 原创文章|
未经许可禁止转载、摘编、复制及镜像等使用
文章转载自 每经网